Forma Farmacéutica y Formulación
Forma Farmacéutica
Tabletas
Composición Cualitativa y Cuantitativa
Cada tableta recubierta de VIDARTIL M 50/500mg contiene:
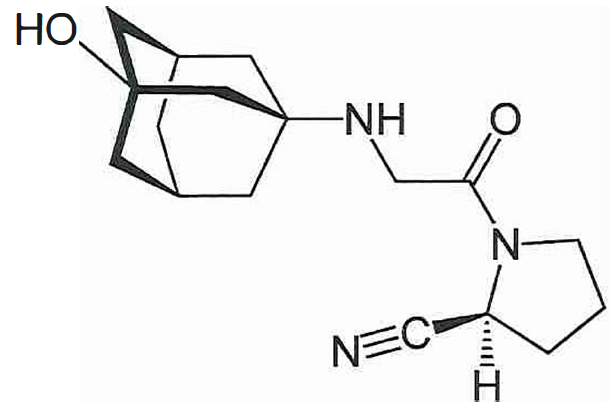
Vildagliptina ………………………………………………………………………………………………………. 50 mg
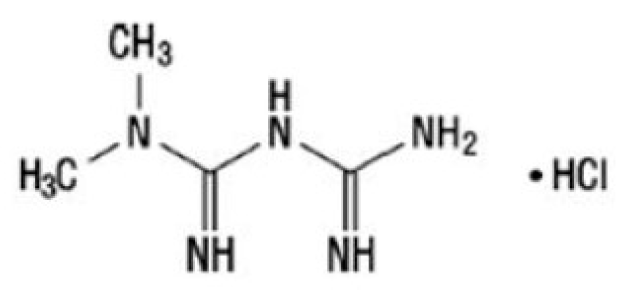
Metforrnina clorhidrato ……………………………………………………………………………………………. 500 mg
Excipientes c.s.p
Cada tableta recubierta de VIDARTIL M 50/850mg contiene:
Vildagliptina ……………………………………………………………………………………………………….50 mg
Metforrnina clorhidrato ……………………………………………………………………………………………. 850 mg
Excipientes c.s.p
Cada tableta recubierta de VIDARTIL M 50/1000mg contiene:
Vildagliptina ………………………………………………………………………………………………………50 mg
Metforrnina clorhidrato …………………………………………………………………………………………… 1000 mg
Excipientes c.s.p
DATOS CLÍNICOS
Indicaciones terapéuticas
Vidartil® M está indicado como adyuvante de la dieta y el ejercicio para mejorar el control glucémico en adultos con diabetes mellitus tipo 2:
En pacientes que no se contralan adecuadamente con hidrocloruro de metformina en monoterapia.
En pacientes que ya están siendo tratados con la combinación de Vildagliptina e hidrocloruro de Metformina, con comprimidos individuales.
En combinación con otros medicamentos para el tratamiento de la diabetes, incluida la insulina, cuando éstos no proporcionan un control glucémico adecuado.
Posología y forma de administración
Posología:
La dosis del tratamiento antihiperglucémico con Vidartil® M debe individualizarse basándose en la pauta posológica actual del paciente, su eficacia y tolerancia, sin superar la dosis diaria máxima recomendada de 100 mg de vildagliptina. El tratamiento con Vidartil® M puede iniciarse con dos comprimidos diarios de 50 mg/850 mg o de 50 mg/1000 mg, uno por la mañana y otro por la noche.
Para pacientes controlados inadecuadamente con su dosis máxima tolerada de metformina en monoterapia: La dosis inicial habitual de Vidartil® M consiste en 50 mg de vildagliptina dos veces al día (100 mg de dosis diaria total) junto con la dosis de Metformina que ya esté tomando el paciente.
Para pacientes que cambian desde la administración conjunta de Vildagliptina y Metformina en
comprimidos separados:
Vidartil® M debe iniciarse a la dosis de vildagliptina y Metformina que ya estuvieran tomando.
Para pacientes controlados inadecuadamente con terapia de combinación dual con Metformina junto con una sulfonilurea:
La dosis de Vidartil® M consiste en 50 mg de vildagliptina dos veces al día (dosis total diaria de 100 mg) y una dosis de Metformina similar a la que ya se estaba tomando el paciente. Cuando Vidartil® M se usa en combinación con una sulfonilurea, puede ser necesaria una dosis menor de la sulfonilurea para reducir el riesgo de hipoglucemia.
Para pacientes controlados inadecuadamente con la terapia de combinación dual compuesta por insulina y la dosis máxima tolerada de Metformina:
La dosis de Vidartil® M consiste en 50 mg de vildagliptina dos veces al día (dosis total diaria de 100 mg) y una ina similar a la que ya se estaba tomando el paciente.
Vidartil M 50mg/500mg está indicado como complemento de la dieta y el ejercicio para mejorar el control glucémico en pacientes cuya diabetes no se controla adecuadamente con clorhidrato de metformina sola o que ya están tratados con la combinación de vildagliptina y clorhidrato de metformina, en tabletas separadas. No se debe iniciar el tratamiento con esta combinación de dosis fija.
Vidartil M 50mg/850mg está indicado en combinación con una sulfonilurea (es decir, terapia de combinación triple) como complemento de la dieta y el ejercicio en pacientes no controlados adecuadamente con Metformina y una sulfonilurea.
Vidartil M 50mg/1000mg está indicado como complemento de la insulina como complemento de la dieta y el ejercicio para mejorar el control glucémico en pacientes cuando una dosis estable de insulina y Metformina por sí solas no proporcionan un control glucémico adecuado.
DOSIS Y VÍAS DE ADMINISTRACIÓN
Para minimizar el riesgo de acidosis l ctica, solo se debe prescribir y usar una concentraci n de Vidartil M
50mg/500mg a la vez. Tambi n se debe advertir a los pacientes que descarten su medicaci n previa con metformina
cuando inicien el tratamiento con Vidartil M 50mg/500mg.
Adultos:
El uso de la terapia antihipergluc mica en el tratamiento de la diabetes tipo 2 debe individualizarse sobre la base
de la eficacia y la tolerabilidad. La dosis inicial recomendada de Vidartil M 50mg/500mg debe basarse en el
r gimen actual de vildagliptina y/o clorhidrato de metformina del paciente. Vidartil M 50mg/500mg debe
administrarse con las comidas para reducir los efectos secundarios gastrointestinales asociados con el clorhidrato
de metformina. Cuando se utiliza Vidartil M 50mg/500mg, no se debe exceder la dosis m xima diaria de
vildagliptina (100 mg).
Dosis inicial para pacientes no controlados adecuadamente con clorhidrato de metformina en monoterapia:
En base a la dosis actual de clorhidrato de metformina del paciente, Vidartil M 50mg/500 puede iniciarse en tabletas
de 50 mg/500 mg, 50 mg/850 mg o 50 mg/1000 mg dos veces al d a.
Dosis inicial para pacientes que cambian del tratamiento combinado de vildagliptina m s clorhidrato de
Metformina en tabletas separadas:
Vidartil M 50mg/500mg puede iniciarse con las tabletas de 50 mg/500 mg, en funci n de la dosis de vildagliptina
o Metformina que ya se est tomando.
Usar en combinaci n con una sulfonilurea o con insulina:
La dosis de Vidartil M 50mg/500mg debe proporcionar vildagliptina en dosis de 50 mg dos veces al d a (dosis
diaria total de 100 mg) y una dosis de Metformina similar a la dosis que ya se est tomando.
Poblaciones especiales
Insuficiencia renal
Se debe evaluar una TFG (Tasa de filtraci n glomerular) antes de iniciar el tratamiento con productos que contienen
Metformina (como Vidartil M 50mg/500mg) y, a partir de entonces, al menos una vez al a o. En pacientes con
mayor riesgo de progresi n adicional de insuficiencia renal y en ancianos, la funci n renal debe evaluarse con m s
frecuencia, p. Ej. cada 3 a 6 meses.
La dosis m xima diaria de Metformina debe dividirse preferiblemente en 2 a 3 dosis diarias. Se deben revisar los
factores que pueden aumentar el riesgo de acidosis l ctica (Advertencias y precauciones de uso especiales) antes
de considerar el inicio de productos que contienen Metformina (como Vidartil M 50mg/500mg) en pacientes con
TFG <60 ml / min. Vidartil M 50mg/500mg est contraindicado en pacientes con TFG <30 ml / min debido a su
componente Metformina (Contraindicaciones).
Contraindicaciones
- Hipersensibilidad a los principios activos o a alguno de los excipientes incluidos. Cualquier tipo de acidosis metabólica aguda (como acidosis láctica, cetoacidosis diabética)
- Pre-coma diabético
- insuficiencia renal grave (TFG < 30 ml/min)
- Trastornos agudos que potencialmente puedan alterar la función renal, tales como:
- deshidratación,
- infección grave,
- shock,
- administración intravascular de medios de contraste yodados (ver sección 4.4). Enfermedad crónica o aguda que pueda causar hipoxia tisular, como:
- insuficiencia cardiaca o respiratoria,
- infarto de miocardio reciente,
- shock.
- Insuficiencia hepática
- Intoxicación
- Lactancia
ADVERTENCIAS Y PRECAUCIONES DE USO ESPECIALES
General
Vidartil M 50mg/500mg no sustituye a la insulina en pacientes que necesitan insulina. Vidartil M 50mg/500mg no debe usarse en pacientes con diabetes Tipo 1 o para el tratamiento de la cetoacidosis diabética.
Monitorización de la función renal
La TFG debe evaluarse antes de iniciar el tratamiento y posteriormente con regularidad (Dosis y forma de administración). Vidartil M 50mg/500mg está contraindicado en pacientes con TFG <30 ml/min debido a su componente Metformina y debe suspenderse temporalmente en presencia de condiciones que alteren la función renal (Contraindicaciones). Se sabe que el clorhidrato de Metformina se excreta sustancialmente por el riñón y el riesgo de acumulación de clorhidrato de Metformina y acidosis láctica aumenta con el grado de deterioro de la función renal. Los pacientes con niveles de creatinina sérica por encima del LSN (límite superior normal) para su edad no deben recibir Vidartil M 50mg/500mg. Dado que la edad avanzada se asocia con una función renal reducida, los productos que contienen Metformina (como Vidartil M 50mg/500mg) deben titularse cuidadosamente
en los ancianos para establecer la dosis mínima para un efecto glucémico adecuado, y la función renal debe controlarse regularmente (ver Contraindicaciones, Dosis y forma de administración).
Medicamentos concomitantes que pueden afectar la función renal o clorhidrato de Metformina Disposición
Los medicamentos concomitantes que pueden afectar la función renal, producir un cambio hemodinámico
significativo o inhibir el transporte renal y aumentar la exposición sistémica de Metformina deben usarse con precaución (ver interacciones con otros medicamentos y otras formas de interacción).
Falla cardíaca
Vidartil M 50mg/500mg está contraindicado en pacientes con insuficiencia cardíaca congestiva que requieren tratamiento farmacológico, que puede interactuar potencialmente con el clorhidrato de Metformina (ver Contraindicaciones e Interacciones con otros medicamentos y otras formas de interacciones).
Uso en insuficiencia hepática
Vildagliptina y, por lo tanto, Vidartil M 50mg/500mg no se recomiendan en pacientes con evidencia clínica o de laboratorio de insuficiencia hepática, incluidos los pacientes con ALT o AST previo al tratamiento> 2.5 veces el LSN.
Dado que la función hepática alterada se ha asociado con algunos casos de acidosis láctica (un riesgo asociado con el clorhidrato de Metformina), los productos que contienen Metformina (como Vidartil M 50mg/500mg) generalmente deben evitarse en pacientes con evidencia clínica o de laboratorio de enfermedad hepática.
Monitoreo de enzimas hepáticas
Estudios de referencia no han notificado casos raros de disfunción hepática (incluida hepatitis) con Vildagliptina. En estos casos, los pacientes estaban generalmente asintomáticos sin secuelas clínicas y las pruebas de función hepática (LFT) volvieron a la normalidad después de la interrupción del tratamiento. Las pruebas de función hepática deben realizarse antes de iniciar el tratamiento con Vidartil M 50mg/500mg. No se recomienda Vidartil M 50mg/500mg en pacientes con una ALT o AST previa al tratamiento> 2.5 veces el LSN. Las PFH deben controlarse durante el tratamiento con Vidartil M 50mg/500mg a intervalos de tres meses durante el primer año y periódicamente a partir de entonces. Los pacientes que desarrollen niveles elevados de transaminasas deben ser controlados con una segunda evaluación de la función hepática para confirmar el hallazgo y, posteriormente, se les debe realizar un seguimiento con pruebas frecuentes de la función hepática hasta que la anomalía / anomalías regresen a la normalidad. Si persiste un aumento de AST o ALT de 3 veces el LSN o más, se recomienda suspender el tratamiento con Vidartil M 50mg/500mg. Los pacientes que desarrollen ictericia u otros signos que sugieran disfunción hepática deben interrumpir el tratamiento con Vidartil M 50mg/500mg y comunicarse con su médico de inmediato. Tras la interrupción del tratamiento con Vidartil M 50mg/500mg y la normalización de LFT, no se debe reiniciar Vidartil M 50mg/500mg. No se recomienda Vidartil M 50mg/500mg en pacientes con insuficiencia hepática.
Acidosis láctica
La acidosis láctica es una complicación metabólica muy rara pero grave que ocurre con mayor frecuencia con un empeoramiento agudo de la función renal, enfermedad cardiorrespiratoria o sepsis. La acumulación de Metformina ocurre con un empeoramiento agudo de la función renal y aumenta el riesgo de acidosis láctica.
En caso de deshidratación (por ejemplo, debido a diarrea o vómitos intensos, fiebre o disminución de la ingesta de líquidos), el paciente debe dejar de tomar productos que contengan Metformina (como Vidartil M 50mg/500mg) y
buscar atención médica inmediata.
Los medicamentos que pueden alterar de forma aguda la función renal (como antihipertensivos, diuréticos y AINE) deben iniciarse con precaución en pacientes tratados con productos que contienen Metformina (como Vidartil M 50mg/500mg). Otros factores de riesgo para la acidosis láctica son la ingesta excesiva de alcohol, insuficiencia hepática, diabetes mal controlada, cetosis, ayuno prolongado y cualquier condición asociada con hipoxia, así como el uso concomitante de medicamentos que pueden causar acidosis láctica (ver Contraindicaciones e Interacciones con otros medicamentos y otras formas de interacción).
Diagnóstico de acidosis láctica
Se debe informar a los pacientes y/o profesionales de la salud del riesgo de acidosis láctica. La acidosis láctica se caracteriza por disnea acidótica, dolor abdominal, calambres musculares, astenia e hipotermia seguidas de coma. Si se sospechan síntomas, el paciente debe dejar de tomar productos que contengan Metformina (como Vidartil M 50mg/500mg) y buscar atención médica inmediata. Los hallazgos de laboratorio de diagnóstico son disminución del pH sanguíneo (<7.35), aumento de los niveles plasmáticos de lactato (> 5 mmol/L) y aumento del desequilibrio aniónico y de la relación lactato / piruvato. Si se sospecha acidosis metabólica, se debe interrumpir el tratamiento con productos que contienen Metformina (como Vidartil M 50mg/500mg) y se debe hospitalizar al paciente de inmediato (ver Sobredosis).
Administración de materiales de contraste yodados intravasculares
La administración intravascular de agentes de contraste yodados puede provocar nefropatía inducida por el contraste, lo que da como resultado la acumulación de Metformina y un mayor riesgo de acidosis láctica.
Los productos que contienen Metformina (como Vidartil M 50mg/500mg) deben suspenderse antes o en el momento de los procedimientos de diagnóstico por imágenes y no deben reiniciarse hasta 48 horas después del procedimiento y deben reiniciarse solo después de que se haya reevaluado la función renal y se haya comprobado que es estable (ver Dosis y forma de administración e Interacciones con otros medicamentos y otras formas de interacción).
Estados hipóxicos
El colapso cardiovascular (shock), la insuficiencia cardíaca congestiva aguda, el infarto agudo de miocardio y otras afecciones caracterizadas por hipoxemia se han asociado con acidosis láctica y también pueden causar insuficiencia renal. Si tales eventos ocurren en pacientes que reciben productos que contienen Metformina (como Vidartil M 50mg/500mg), el medicamento debe suspenderse de inmediato.
Procedimientos quirúrgicos
Los productos que contienen Metformina (como Vidartil M 50mg/500mg) deben suspenderse en el momento de la cirugía bajo anestesia general, espinal o epidural (excepto procedimientos menores no asociados con una ingesta restringida de alimentos y líquidos) y pueden reiniciarse no antes de las 48 horas posteriores a la cirugía o hasta que se haya reanudado la nutrición oral del paciente y se haya reevaluado la función renal y se haya comprobado que es estable.
Consumo de alcohol
Se sabe que el alcohol potencia el efecto del clorhidrato de metformina sobre el metabolismo del lactato. Se debe advertir a los pacientes contra la ingesta excesiva de alcohol mientras reciben productos que contienen metformina
(como Vidartil M 50mg/500mg).
Hipoglucemia
La hipoglucemia no suele ocurrir en pacientes que reciben Vidartil M 50mg/500mg, pero podría ocurrir cuando la ingesta calórica es deficiente, cuando el ejercicio extenuante no se compensa con la suplementación calórica o el uso de etanol. Los pacientes ancianos, debilitados o desnutridos y aquellos con insuficiencia suprarrenal o pituitaria o intoxicación por alcohol son susceptibles a efectos hipoglucemiantes. La hipoglucemia puede ser difícil de reconocer en personas de edad avanzada y en personas que toman fármacos bloqueadores betaadrenérgicos.
Pérdida de control de la glucosa en sangre
Cuando un paciente estabilizado con cualquier régimen para diabéticos se expone a estrés como fiebre, trauma, infección, cirugía, etc., puede ocurrir una pérdida temporal del control glucémico. En esos momentos, puede ser necesario suspender Vidartil M 50mg/500mg y administrar insulina temporalmente. Vidartil M 50mg/500mg puede reiniciarse una vez resuelto el episodio agudo.
Artralgia
Informes de referencia reportaron dolor articular, que puede ser intenso, en pacientes que toman inhibidores de la DPP-4. La aparición de los síntomas después del inicio del tratamiento puede ser rápida o puede ocurrir después de períodos más prolongados. Se debe considerar la interrupción del tratamiento en pacientes que presenten o experimenten una exacerbación de los síntomas articulares durante el tratamiento con inhibidores de la DPP-4.
EFECTOS ADVERSOS (EFECTOS NO DESEADOS)
Notificación de sospechas de efectos adversos
Es importante notificar las sospechas de reacciones adversas después del registro del medicamento. Permite un seguimiento continuo de la relación beneficio-riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas en Farmacovigilancia Luminovapg farmacovigilancia@luminovapg.com
Los datos presentados aquí se refieren a la administración de Vildagliptina y metformina como una combinación de dosis libre o fija.
Se han registrado casos raros de angioedema con Vildagliptina a una tasa similar a los controles. Se registró una mayor proporción de casos cuando se administró Vildagliptina en combinación con un inhibidor de la enzima convertidora de angiotensina (inhibidor de la ECA). La mayoría
Sobredosis
No hay datos disponibles sobre la sobredosis de Vidartil M®.
Vildagliptina
La información sobre la sobredosis de vildagliptina es limitada.
Síntomas
Se ha obtenido información sobre los síntomas probables en caso de sobredosis a partir de un estudio de tolerabilidad con dosis crecientes de vildagliptina en voluntarios sanos durante 10 días. Con 400 mg se observaron tres casos de dolor muscular y casos individuales de parestesia leve y transitoria, fiebre, edema y un aumento transitorio de los niveles de lipasa. Con 600 mg se observó un caso de edema en pies y manos y aumentos en los niveles de creatinina fosfokinasa (CPK), AST, proteína C-reactiva (CRP) y mioglobina.
Otros tres sujetos experimentaron edema en los pies, con parestesia en dos casos. Tras interrumpir la administración del medicamento en estudio, todos los síntomas y los valores de laboratorio anormales se resolvieron sin necesidad de tratamiento.
Metformina
Una sobredosis masiva de Metformina (o si existe riesgo de acidosis láctica) puede dar lugar a acidosis láctica, lo que es una urgencia médica y debe tratarse en un hospital.
Tratamiento
El método más eficaz para eliminar Metformina es la hemodiálisis. Sin embargo, vildagliptina no puede eliminarse por hemodialisis, pero sí su principal metabolito de hidrólisis (LAY 151). Se recomienda un tratamiento de soporte.
PROPIEDADES FARMACOLÓGICAS
Propiedades farmacodinámicas
Mecanismo de acción
Vidartil® M combina dos fármacos antidiabéticos con mecanismos de acción complementarios para mejorar el control glucémico en pacientes con diabetes tipo 2: vildagliptina, un miembro del grupo de los potenciadores de los islotes pancreáticos, e Hidrocloruro de Metformina, un miembro del grupo de las biguanidas.
Vildagliptina, un miembro del grupo de los potenciadores de los islotes pancreáticos, es un inhibidor potente y selectivo de la dipeptidil peptidasa 4 (DPP-4). Metformina actúa principalmente disminuyendo la producción hepática endógena de glucosa.
Efectos farmacodinámicos
Vildagliptina
Vildagliptina actúa principalmente inhibiendo la dipeptidil peptidasa 4 (DPP-4), un enzima responsable de la degradación de las hormonas incretinas GLP-1 (péptido 1 similar al glucagón) y GIP (polipéptido insulinotrópico dependiente de glucosa).
La administración de vildagliptina da lugar a una inhibición rápida y completa de la actividad de la DPP-4, lo que origina un aumento de los niveles endógenos post-prandiales y en ayunas de las hormonas incretinas GLP-1 y GIP.
Mediante el aumento de los niveles endógenos de las hormonas incretinas, vildagliptina potencia la sensibilidad a la glucosa de las células beta, favoreciendo la secreción de insulina dependiente de glucosa. El tratamiento con dosis de vildagliptina de 50-100 mg al día en pacientes con diabetes tipo 2 mejoró de forma significativa los marcadores de la función de las células beta, incluyendo el HOMA- (Homeostasis Model Assessment-ß), el cociente proinsulina/insulina y las medidas de sensibilidad de las células beta en el test de tolerancia a la comida con muestreo múltiple. En individuos no diabéticos (glucemia normal), vildagliptina no estimula la secreción de insulina ni reduce los niveles de glucosa.
Mediante el aumento de los niveles de GLP-1, vildagliptina también potencia la sensibilidad de las células alfa a la glucosa, adecuando mejor la secreción de glucagón en función de la glucosa.
Al aumentar los niveles de la hormona incretina y con ello potenciar el aumento del cociente insulina/glucagón durante la hiperglucemia, disminuye la liberación hepática de glucosa en la fase post-prandial o en ayunas, consiguiendo una reducción de la glucemia.
El efecto de retraso sobre el vaciado gástrico, conocido cuando aumentan los niveles de GLP-1, no se observa con el tratamiento con vildagliptina.
Metformina
Metformina es una biguanida con efectos antihiperglucemiantes que disminuye la glucosa plasmática basal y post- prandial. No estimula la producción de insulina y por lo tanto no produce hipoglucemia ni un aumento del peso corporal.
Metformina puede disminuir la glucemia mediante tres mecanismos:
- reducción de la producción hepática de glucosa por la inhibición de la gluconeogénesis y glucogenolisis;
- en músculo, incrementando moderadamente la sensibilidad a la insulina, mejorando la captación y utilización de la glucosa periféricas;
- retrasando la absorción de glucosa intestinal.
Metformina estimula la síntesis de glucógeno intracelular al actuar sobre la glucógeno sintasa y aumenta la capacidad de transporte de tipos específicos de transportadores de membrana de la glucosa (GLUT-1 y GLUT-4).
En humanos, independientemente de su acción sobre la glucemia, Metformina tiene efectos favorables sobre el metabolismo lipídico. Esto se ha demostrado a dosis terapéuticas en ensayos clínicos controlados a medio o largo plazo: Metformina reduce los niveles séricos de colesterol total, LDL colesterol y triglicéridos.
Propiedades farmacodinámicas
Absorción
La ingesta de comida no tiene efecto sobre la magnitud y velocidad de absorción de Vildagliptina a partir de los comprimidos de Vidartil® M.
A continuación se presentan las propiedades farmacocinéticas de los principios activos individuales de Vidartil® M.
Vildagliptina
Absorción
Tras la administración de una dosis por vía oral en ayunas, vildagliptina se absorbe rápidamente y se observan concentraciones plasmáticas máximas a las 1,7 horas. La comida retrasa ligeramente el tiempo para alcanzar la concentración plasmática máxima a las 2,5 horas, pero no modifica la exposición global (AUC). La administración de vildagliptina con la comida da lugar a una disminución de la Cmax (19%) en comparación con la administración en ayunas. Sin embargo, la magnitud del cambio no es clínicamente significativa, por ello vildagliptina puede administrarse con o sin comida. La biodisponibilidad absoluta es del 85%.
Distribución
La unión a proteínas plasmáticas de vildagliptina es baja (9,3%) y vildagliptina se distribuye equitativamente entre el plasma y los eritrocitos. El volumen de distribución medio de vildagliptina en estado estacionario tras la administración intravenosa (Vss) es 71 litros, lo que sugiere una distribución extravascular.
Biotransformación
El metabolismo es la principal vía de eliminación de vildagliptina en humanos, afectando a un 69% de la dosis. El metabolito principal (LAY 151), farmacológicamente inactivo, se obtiene por hidrólisis del grupo ciano y representa un 57% de la dosis, seguido del producto de la hidrólisis amídica (4% de la dosis). La DPP-4 participa parcialmente en la hidrólisis de vildagliptina, según un estudio in vivo en ratas con deficiencia en DPP-4. Vildagliptina no se metaboliza por las enzimas del CYP 450 en grado cuantificable alguno. En consecuencia, no es previsible que el aclaramiento metabólico de vildagliptina se vea afectado por la administración concomitante de medicamentos que sean inhibidores o inductores de las enzimas del CYP 450. Estudios de referencia realizados in vitro han demostrado que vildagliptina no inhibe/induce las enzimas del CYP 450. Por ello, no es probable que vildagliptina afecte al aclaramiento metabólico de medicamentos administrados concomitantemente y metabolizados por las isoenzimas CYP 1A2, CYP 2C8, CYP 2C9, CYP 2C19, CYP 2D6, CYP 2E1 o CYP 3A4/5.
Eliminación
Tras la administración por vía oral de vildagliptina, aproximadamente el 85% de la dosis se excretó en la orina y el 15% de la dosis se recuperó en las heces. La excreción renal de vildagliptina inalterada representó un 23% de la dosis administrada por vía oral. Tras la administración intravenosa a sujetos sanos, el aclaramiento plasmático total y renal de vildagliptina es de 41 y 13 l/h, respectivamente. La semivida de eliminación tras la administración intravenosa es de aproximadamente 2 horas. La semivida de eliminación tras la administración oral es de aproximadamente 3 horas.
Metformina
Absorción
Tras la administración oral de una dosis de Metformina, la concentración plasmática máxima (Cmax) se alcanza después de unas 2,5 h (tmax). La biodisponibilidad absoluta de un comprimido de 500 mg de
Metformina es aproximadamente del 50-60% en sujetos sanos. Tras la administración oral de una dosis, la fracción no absorbida recuperada en heces fue del 20-30%.
Tras la administración oral, la absorción de Metformina es saturable e incompleta. Se asume que la farmacocinética de la absorción de Metformina es no lineal. Con las dosis y pautas posológicas habituales de Metformina, las concentraciones plasmáticas en estado estacionario se alcanzan entre las 24-48 h y generalmente son inferiores a 1 mg/mL. En ensayos clínicos controlados, los niveles plasmáticos máximos de Metformina (Cmax) no excedieron de
La ingesta de alimentos retrasa ligeramente y disminuye la magnitud de la absorción de metformina.
Distribución
La unión a proteínas plasmáticas es insignificante. Metformina se distribuye en los eritrocitos. El volumen de distribución medio (Vd) oscila entre 63-276 litros.
Biotransformación
Metformina se excreta inalterada en la orina. No se han identificado metabolitos en humanos.
Eliminación
Metformina se elimina por excreción renal. El aclaramiento renal de Metformina es > 400 ml/min, lo que indica que Metformina se elimina por filtración glomerular y secreción tubular. Tras la administración de una dosis oral, la semivida de eliminación terminal aparente es de aproximadamente 6,5 h. En caso de insuficiencia renal, el aclaramiento renal disminuye proporcionalmente al aclaramiento de creatinina y, por lo tanto, se prolonga la semivida de eliminación, dando lugar a un aumento de los niveles plasmáticos de Metformina.
DATOS FARMACÉUTICOS
Comercial: Vidartil M 50 mg/ 500 mg. caja con 30 y 60 tabletas recubiertas con inserto.
Comercial: Vidartil® M 50/850 mg. Caja con 30 y 60 tabletas recubiertas con inserto.
Comercial: Vidartil® M 50/1000 mg. Caja con 30 y 60 tabletas recubiertas con inserto
Precauciones especiales de conservación
Manténgase fuera del alcance de los niños. Consérvese en un lugar seco, protegido de la luz y el calor. Venta bajo
prescripción médica. Temperatura de almacenamiento: No mayor de 30ºC.
TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Titular: Unipharm, S.A.
Fabricante: Unipharm, S.A. / Guatemala
REFERENCIAS BIBLIOGRÁFICAS
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos https://www.ema.europa.eu/en/documents/product-information/zomarist-epar-product- information_en.pdf (Revisión Mayo 2020].
La información detallada de este medicamento está disponible en la página web de la Agencia Española de Medicamentos y Productos Sanitarios. Cambios de especial interés en medicamentos ya autorizados. Nuevas indicaciones/Modificación de Indicaciones https://www.aemps.gob.es/informa/boletines-aemps/boletin- chmp/2021-boletin-chmp/reunion-del-comite-de-medicamentos-de-uso-humano-chmp-de-mayo-2021/ (Revisión Junio 2021].
Referencia propiedades físico-químicas https://pubchem.ncbi.nlm.nih.gov/compound/Galvus#section=2D-Structure
https://pubchem.ncbi.nlm.nih.gov/compound/Metformin-hydrochloride#section=Computed-Properties
REFERENCIAS BIBLIOGRÁFICAS
- Ema.europa.eu. 2012. FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSITCAS DEL PRODUCTO.. (online) Disponible en: <https://www.ema.europa.eu/en/documentos/overview/galvus-epar-summary-public_en.pdf> Revisión 24 de agosto de 2020
- Martindale. Guía completa de Consulta Farmacoterapéutica. 38ª Edición. Pharma Editores, S.L. Barcelona 2014. pp504-505.