Forma Farmacéutica y Formulación
Forma Farmacéutica
Granulado para suspensión oral
Composición Cualitativa y Cuantitativa
Cada 5ml de suspensión reconstituida contiene:
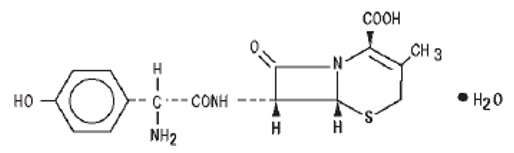
Cefadroxilo monohidrato equivalente a cefadroxilo base…250.00 mg
Vehículo c.s.p.
PROPIEDADES FARMACOLÓGICAS
a. FARMACODINÁMICAS:
Descripción: es un antibiótico cefalosporinico semi sintético destinado para la administración oral. Es soluble en agua y estable en medio ácido.
Microbiología: Las cefalosporinas son bactericidas debido a que causan inhibición en la síntesis de la pared celular. Cefadroxil ha demostrado ser activo contra los siguientes microorganismos tanto en in vitro como en infecciones clínicas:
- Streptococcus beta- hemolitico
- Staphylococcus, incluyendo las cepas productoras de penicilinasa
- Streptococcus (Diplococcus) pneumoniae
- Escherichia coli
- Especies de Klebsiella
- Moraxella (Branhamella) catarrhalis
Nota: La mayoría de las cepas de Enterococcus faecalis (anteriormente Streptococcus faecalis) y Enterococcus faecium (anteriormente Streptococcus faecium) son resistentes. No es activa contra la mayoría de las cepas de especies de Enterobacter, Morganella morganii (anteriormente Proteus morganii), y P. vulgaris, no tiene actividad contra especies de Pseudomonas y Acinetobacter calcoaceticus (anteriormente Mima y especies de Herellea).
b. FARMACOCINÉTICAS:
Farmacología clínica: Es rápidamente absorbida después de la administración oral. Después de dosis únicas de 500mg y 1000mg los picos de concentración sérica promedio fueron aproximadamente 16 y 28µg/mL, respectivamente. Concentraciones medibles estuvieron presentes después de 12 horas de administración. Más del 90% del medicamento se excreta por la orina sin cambios en menos de 24 horas. Los picos de concentración en orina son aproximadamente 1800µg/mL durante un periodo posterior a la dosis única de 500mg. El aumento en la dosis generalmente produce aumentos proporcionales en la concentración urinaria.
DATOS CLÍNICOS
a. INDICACIONES TERAPÉUTICAS:
Está indicado para el tratamiento de pacientes con infecciones causadas por cepas susceptibles de los organismos designados en las siguientes enfermedades:
- Infecciones del tracto urinario causadas por coli, P. mirabilis y especies de Klebsiella.
- Infecciones de la piel y de las estructuras de la piel causadas por estafilocos y/o estreptococos.
- Faringitis y/o amigdalitis causada por Streptococcus pyogenes (Grupo A Estreptococo beta-hemolítico).
Nota: Es generalmente efectiva en la erradicación de estreptococos de la orofaringe.
b. POSOLOGÍA Y FORMA DE ADMINISTRACIÓN:
Calcular 30mg/kg/24 horas dividido cada 12 horas, o:
De 1 a 6 años: 1 cucharadita (5ml) cada 12 horas
De 6 a 12 años: 2 cucharaditas (10ml) cada 12 horas
Insuficiencia renal
En pacientes con insuficiencia renal, la dosis de monohidrato de cefadroxilo debe ser ajustada de acuerdo con las tasas de eliminación de creatinina para evitar la acumulación de fármacos. Pacientes con eliminación de creatinina mayores de 50mL/min pueden ser tratados como si fueran pacientes con una función renal normal.
c. CONTRAINDICACIONES:
Contraindicado en pacientes con alergias conocidas al grupo de los antibióticos cefalosporinas.
d. ADVERTENCIAS Y PRECAUCIONES:
Antes de administrar la terapia, debe realizarse una consulta cuidadosa para determinar si el paciente ha tenido reacciones anteriores de hipersensibilidad a cefadroxilo, cefalosporinas, penicilinas u otros medicamentos. Si este producto debe darse a pacientes sensibles a penicilina, se deberá tomar precauciones por la sensibilidad cruzada entre antibióticos beta lactamicos, ha sido ampliamente documentada y puede ocurrir en el 10% de pacientes con historia de alergias a la penicilina.
Si ocurre una reacción alérgica, descontinúe el medicamento. Reacciones graves de hipersensibilidad aguda pueden requerir tratamiento con epinefrina y otras medidas de emergencia, incluyendo oxígeno, fluidos intravenosos, antihistaminos intravenosos, corticosteroides, aminas para la presión y manejo de las vías respiratorias.
Se ha reportado colitis pseudomembranosa con casi todos los agentes antibacterianos, incluyendo cefadroxilo, y puede variar desde leve hasta poner en peligro la vida. Por lo tanto, es importante considerar este diagnóstico en pacientes que presentan diarrea posterior a la administración de los agentes antibacterianos.
El tratamiento con agentes antibacterianos altera la flora normal del colon y puede permitir el crecimiento excesivo de clostridia. Estudios han indicaron que es una toxina producida por Clostridium difficile, es una causa primaria de “colitis asociada a antibióticos”.
Después de establecido el diagnóstico de colitis pseudomembranosa, deben iniciarse medidas terapéuticas. Los casos leves de colitis pseudomembranosa generalmente responden a la interrupción del medicamento. En los casos de moderados a severos, se debe considerar la administración de líquidos y electrolitos, suplementos de proteínas y el tratamiento con fármaco antibacteriano eficaz contra Clostridium difficile.
Debe usarse con precaución en presencia de función renal notablemente alterada (tasa de aclaramiento de creatinina de menos de 50 ml/ min/ 1.73 M2). En pacientes con conocimiento o sospecha de insuficiencia renal, deben realizarse observación clínica cuidadosa y estudios de laboratorio apropiados antes y durante la terapia.
El uso prolongado puede provocar el crecimiento excesivo de organismos no susceptibles. Es esencial la observación cuidadosa del paciente. Si se produce una sobreinfección durante la terapia, se deben tomar medidas apropiadas. Debe prescribirse con precaución en personas con antecedentes de enfermedades gastrointestinales, particularmente colitis.
Forma de preparación: Agitar el envase para desprender el contenido. Agregar agua hervida y fría, hasta cubrir el granulado, agitar bien completar con agua hasta donde indica la flecha (65mL). Agitar bien antes de usar.
Información importante sobre excipientes: Este medicamento contiene azúcar refinada, los pacientes con intolerancia hereditaria a la fructosa, insuficiencia sacarasa-isomaltasa o malabsorción de glucosa o galactosa no deben tomar este medicamento. Este medicamento contiene sodio, debe tenerse en cuenta en los pacientes con una dieta baja en sodio. Contiene color amarillo F.D.&C, #6, este medicamento puede producir reacciones alérgicas, puede provocar asma, especialmente en pacientes alérgicos al ácido acetilsalicílico.
e. INTERACCIONES CON OTROS MEDICAMENTOS:
Pruebas positivas directas de Coombs durante el tratamiento con antibióticos de cefalosporina. En estudios hematológicos o en procedimientos de comparación cruzada transfusionales cuando son realizadas pruebas de antiglobulina secundarias o pruebas de Coombs a los recién nacidos cuyas las madres han recibido antibióticos de cefalosporina antes del parto, se debe
reconocer que una prueba positiva de Coombs puede deberse al medicamento.
f. EMBARAZO Y LACTANCIA:
- embarazo: Categoría B en embarazo, estudios de reproducción en ratones y ratas en dosis de hasta 11 veces la dosis humana y no han revelado evidencia de deterioro de la fertilidad o daño al feto. Sin embargo, no existen estudios adecuados y bien controlados en mujeres embarazadas, este medicamento debe usarse durante el embarazo solo si es claramente
- trabajo de parto y parto: El tratamiento solo debe ser dado si es
- madres lactantes: Se debe tener precaución cuando se administra monohidrato de cefadroxilo a una madre en
g. REACCIONES ADVERSAS:
Gastrointestinal: El inicio de los síntomas de la colitis pseudomembranosa puede ocurrir durante o después del tratamiento con antibióticos. Raramente dispepsia, náuseas y vómitos, también puede aparecer diarrea.
Hipersensibilidad: Alergias (en forma de erupción, urticaria, angioedema y prurito), estas reacciones generalmente se disminuyeron al suspender el medicamento, anafilaxias.
Otros: Otras reacciones han incluido disfunción hepática incluyendo colestasis y elevaciones en transaminasa sérica, prurito genital, moniliasis genital, vaginitis, neutropenia transitoria moderada, fiebre, agranulocitosis, trombocitopenia, insuficiencia hepática idiosincrásica, eritema multiforme, síndrome de Stevens-Johnson, enfermedad del suero y artralgia han sido raramente reportados.
Reacciones adversas y pruebas de laboratorio alteradas para antibióticos de clase cefalosporina: Necrólisis epidérmica tóxica, dolor abdominal, sobreinfección, disfunción renal, nefropatía tóxica, anemia aplásica, anemia hemolítica, hemorragia, tiempo de protrombina prolongado, prueba de Coombs positiva, aumento de BUN, aumento de la creatinina, aumento de fosfatasa alcalina, aumento de aspartato aminotransferasa (AST), aumento de alanina aminotransferasa (ALT), aumento de bilirrubina, aumento de LDH, eosinofilia, pancitopenia, neutropenia.
Varias cefalosporinas han sido implicadas en desencadenar convulsiones, especialmente en pacientes con insuficiencia renal, cuando la dosis no fue reducida. Si las convulsiones están asociadas con la terapia, el medicamento debe suspenderse, la terapia anticonvulsiva se puede administrar si esta clínicamente indicada.
h. SOBREDOSIFICACIÓN:
Niños menores de seis años: la ingestión de menos de 250 mg / kg de las cefalosporinas no están asociadas a resultados significativos. No se requiere ninguna acción aparte del apoyo general y la observación. Para cantidades superiores a 250 mg / kg, induzca el vaciado de la secreción gástrica.
DATOS FARMACÉUTICOS
a. PERÍODO DE VALIDEZ:
36 meses
b. PRECAUCIONES ESPECIALES DE CONSERVACIÓN:
Almacenar a temperatura no mayor de 30°C. La suspensión preparada tiene una duración de 7 días a temperatura ambiente y 14 días en refrigeración.
c. NATURALEZA Y CONTENIDO DEL ENVASE:
Muestra médica:
Caja con frasco de 30 ml
Comercial:
Caja con frasco de 60 ml
Caja con frasco de 80 ml
Hospital:
Caja con 96 unidades de 60 ml
Caja con 96 unidades de 80 ml
FECHA DE REVISIÓN
Octubre – 2018
REFERENCIAS BIBLIOGRÁFICAS
U.S. Food & Drug Administration, recopilado de: https://www.accessdata.fda.gov/drugsatfda_ docs/label/2002/50512s44lbl.pdf