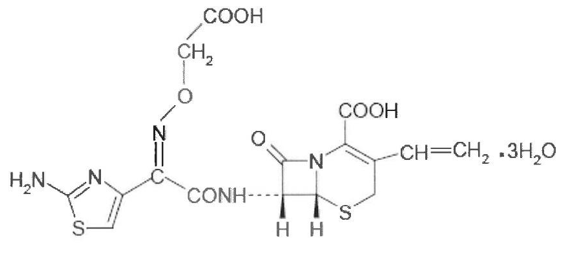
Forma Farmacéutica y Formulación
Forma Farmacéutica
Granulado para suspensión oral
Composición Cualitativa y Cuantitativa
Gránulos para suspensión oral
Cada 5 ml de suspensión reconstituida contiene:
Cefixima trihidrato equivalente a Cefixima…100 mg
Excipientes c.s. p
PROPIEDADES FARMACOLÓGICAS
a. PROPIEDADES FARMACODINÁMICAS:
La cefixima es un antibiótico β- lactámico, de administración oral. Como el resto de β-lactámicos cefalosporínicos, el mecanismo de acción de cefixima es bactericida y se basa en la inhibición de la síntesis de la pared bacteriana. Cefixima es resistente a la mayoría de las β- lactamasas y es activa frente a una amplia gama de microorganismos Gram- positivos y Gram-negativos. Por consiguiente, es activa frente a muchas cepas ampicilin o amoxicilin-resistentes.
Su actividad antibacteriana característica es:
- Cepas normalmente sensibles
Streptococcus pneumoniae y S. pyogenes; Haemophilus influenzae, Branhamella (Moraxella) catarrhalis, E. coli, Proteus mirabilis, K. pneumoniae, Citrobacter sp, Serratia sp.
- Cepas normalmente resistentes
Bacillus subtilis, B. cereus, Streptococcus faecalis, Pseudomonas aeruginosa, P. maltophilia, Listeria monocytogenes, cepas de Staphylococcus, incluyendo los meticilin resistentes, Enterobacter.
- Cepas de sensibilidad variable
Entre los gérmenes sensibles a cefixima, pero, cuya sensibilidad deberá ser comprobada antes del inicio del tratamiento, se encuentran: Streptococcus agalactiae, Neisseria gonorrhoeae, Haemophilus parainfluenzae, Proteus vulgaris, Klebsiella oxytoca, Pasteurella multocida, Especies de Providencia, Salmonella y Shigella.
b. PROPIEDADES FARMACOCINÉTICAS:
El tiempo de vida media de cefixima (T 1/2) es marcadamente más largo que el de otros β-lactámicos orales (media 3,3 horas), lo que posibilita su dosificación en una o dos dosis
Después de una toma única de 200 mg:
- El pico máximo de concentración sérica alcanza de 3 a 3,3 mg/l, entre las 3 y 4 horas tras la
Después de una toma única de 400 mg:
- El pico máximo alcanza los 4,8 mg/l, entre las 3 y 4 horas después de la
- La vida media plasmática es de 3 a 4
El producto se elimina inalterado por vía renal (12 al 20%), y la eliminación extrarrenal se realiza en su mayor parte por vía biliar.
Las concentraciones urinarias se sitúan muy por encima de las CMI de los gérmenes sensibles durante todo el intervalo entre las dos tomas, de acuerdo con la posología recomendada. Debido a que cefixima se absorbe independientemente del pH gástrico, su biodisponibilidad no se ve modificada por las comidas, ni por fármacos antisecretores H2 o antiácidos. En la administración de dosis repetidas de cefixima, los niveles plasmáticos no presentan fenómeno de acumulación. La difusión tisular en el oído medio, amígdalas, epitelio bronquial y parénquima pulmonar es semejante a la de otras cefalosporinas y de amoxicilina.
DATOS CLÍNICOS
a. INDICACIONES TERAPÉUTICAS:
FIXIM® Contiene un medicamento que se llama “cefixima”, que pertenece al grupo de antibióticos de las “cefalosporinas”. Éstos se emplean para el tratamiento de infecciones causadas por bacterias. Está indicada en infecciones de vías respiratorias altas como: faringitis y amigdalitis causadas por Streptococcus pyogenes. Infecciones de las vías respiratorias bajas como: bronquitis aguda, episodios de reagudización de bronquitis crónica y neumonías, causadas por Streptococcus pneumoniae y Haemophilus influenzae. Infecciones ORL: Otitis media causada por Haemophilus influenzae, Branhamella (Moraxella) catarrhalis, Streptococcus pyogenes y Streptococcus pneumoniae. Infecciones de vías urinarias no complicadas causadas por Escherichia coli y Proteus mirabilis.
La penicilina es el fármaco de elección en el tratamiento y profilaxis de las infecciones estreptocócicas, incluyendo la profilaxis de la fiebre reumática. Cefixima es generalmente eficaz en la erradicación de los estreptococos de la orofaringe, sin embargo, no se dispone por el momento de datos que avalen la eficacia de cefixima en la prevención de la fiebre reumática.
b. POSOLOGÍA Y FORMA DE ADMINISTRACIÓN:
La dosis diaria recomendada para adultos y niños mayores de 12 años, o de más de 50 kilos de peso, es de 200 mg/12 h o de 400 mg una vez al día. En niños, la dosis diaria recomendada es de 8 mg/kg/día, en suspensión oral, pudiendo ser administrado en dosis única o en dos dosis de 4 mg/kg/día cada 12 horas.
| Peso corporal del niño | Suspensión oral |
| 6,0 kg | 2,5 ml/día |
| 12,5 kg | 5 ml/día |
| 25,0 kg | 10 ml/día |
| 37,5 kg | 15 ml/día |
| 50,0 kg o adulto | 20 ml/día |
La dosis máxima recomendada no deberá exceder de 12 mg/kg de peso y día.
En mujeres con cistitis aguda no complicada se recomienda una dosis de 400 mg diarios, en toma única, durante 3 días. En caso de insuficiencia renal con un aclaramiento de creatinina ≥ 20 ml/minuto, no es preciso modificar la dosis; si el aclaramiento es inferior, se deberá reducir la dosis a la mitad. En pacientes hemodializados, la posología de cefixima no deberá exceder tampoco los 200 mg/día.
En pacientes con insuficiencia hepática, el hecho de que cefixima no se metabolice en el hígado posibilita la administración del preparado, sin necesidad de modificar la dosis. La adecuación en la dosificación de Cefixima tampoco precisa ser modificada en ancianos.
No se recomienda su administración en prematuros, recién nacidos y lactantes hasta 6 meses por la ausencia de datos sobre el balance riesgo-beneficio en estas condiciones.
c .CONTRAINDICACIONES:
nunca debe ser administrado a pacientes con hipersensibilidad a las cefalosporinas, cefamicinas o a alguno de los
d. ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE EMPLEO:
Antes de la administración del medicamento, debe investigarse en el paciente la posible existencia anterior de manifestaciones de hipersensibilidad a cefalosporinas, a otros antibióticos betalactámicos (por ejemplo, penicilinas), o de un componente alérgico fundamentalmente de naturaleza medicamentosa. La aparición de cualquier manifestación alérgica requiere la suspensión del
Se recomienda especial atención en aquellos pacientes que padecen asma y diátesis alérgica. El uso prolongado de cefixima puede dar lugar a sobreinfección, producida por microorganismos no sensibles (p.ej. Cándida, Enterococos, Clostridium difficile), que pueden requerir la interrupción del tratamiento.
Se han comunicado casos de colitis pseudomembranosa con antibióticos de amplio espectro. Por tanto, es importante considerar su diagnóstico en pacientes que desarrollan diarrea grave en asociación con el uso de los antibióticos. En el caso que se sospeche colitis pseudomembranosa, el tratamiento debe interrumpirse inmediatamente y debe iniciarse el tratamiento correctivo adecuado.
No se recomienda en pacientes con alteraciones gastrointestinales severas que incluyan náuseas y vómitos. Se recomienda precaución en aquellos pacientes tratados simultáneamente con diuréticos (por ejemplo, furosemida) y/o tratados con otros medicamentos potencialmente nefrotóxicos (por ejemplo, antibióticos aminoglucósidos), especialmente en aquellos pacientes que padecen enfermedades subyacentes (por ejemplo, infecciones severas, septicemia), ya que puede producirse isquemia renal. Debido al uso simultáneo de estos medicamentos, puede producirse deficiencia de la función renal o incluso fallo renal agudo. En estos casos, es necesaria la monitorización de la función renal. Se recomienda especial precaución en pacientes con insuficiencia renal severa.
Este medicamento contiene sacarosa (azúcar refinado). Los pacientes con intolerancia hereditaria a la fructosa, insuficiencia sacarasa-isomaltasa o malabsorción de glucosa o galactosa no deben tomar este medicamento.
FORMA DE PREPARACIÓN
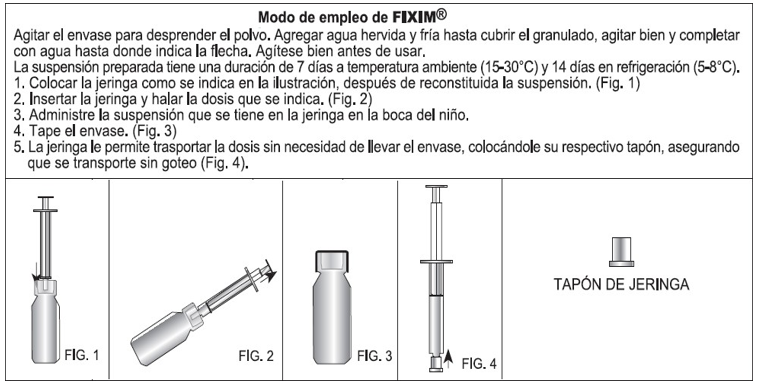
e. INTERACCIONES CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN:
Sustancias potencialmente nefrotóxicas como los antibióticos aminoglucósidos, colistina, polimixina, cloranfenicol o diuréticos potentes (como ácido etacrínico o furosemida): pueden incrementar el riesgo de daño en la función renal.
Bloqueadores de los canales de calcio como el nifedipino: pueden incrementar la biodisponibilidad de la cefixima. No obstante, no se recomienda modificación de la dosis.
Anticoagulantes cumarínicos: pueden aumentar el tiempo de protombina, con o sin hemorragia. Se recomienda la monitorización de los parámetros de coagulación.
Puede dar falsas reacciones positivas en los tests de determinación de cetonas y glucosa en orina cuando la determinación se realiza mediante métodos reductores. No es el caso cuando la determinación se realiza mediante métodos enzimáticos. También puede dar lugar a una falsa reacción de Coombs directo positiva.
f. EMBARAZO Y LACTANCIA:
- Embarazo: no se dispone de datos clínicos, Debido a la limitada experiencia clínica durante el embarazo, no se recomienda su uso en mujeres embarazadas, a menos que el médico así lo considere después de valorar el beneficio-riesgo, especialmente durante el primer trimestre de
- Lactancia: No se ha detectado que la cefixima se excrete por la lecha No se recomienda el uso en mujeres durante la lactancia, a menos que el médico así lo considere después de valorar el beneficio riesgo.
g. EFECTOS SOBRE LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MAQUINARIAS:
No tiene efectos sobre la capacidad para conducir y utilizar máquinas. No obstante, algunas reacciones adversas pueden afectar a la capacidad de concentración y reacción lo que puede suponer un riesgo en aquellas situaciones en las que la concentración y reacción son de vital importancia, por ejemplo, en la conducción o en el uso de máquinas.
h. REACCIONES ADVERSAS:
- Frecuentes: diarrea, heces
- Poco frecuentes: náuseas y vómitos, indigestión, dolores abdominales, urticaria, eritema, exantema, cefalea, aumento transitorio de las enzimas hepáticas en suero (transaminasas, fosfatasas alcalinas).
- Raras: falta de apetito, flatulencias, prurito, inflamación de las mucosas, mareo, fiebre, eosinofilia, reacciones de hipersensibilidad como rubor, palpitaciones, disnea, hipotensión, broncoespasmos, edema angioneurótico, aumento transitorio de la concentración de urea, infecciones por hongos o bacterias resistentes tras la administración continuada (prurito vaginal, vaginitis y candidiasis).
- Muy raras: colitis pseudomembranosa, inflamación del intestino grueso asociado a antibióticos. Necrólisis epidérmica tóxica, Síndrome de Stevens- Johnson, eritema exudativo Multiforme, hiperactividad transitoria, leucopenia, agranulocitosis, pancitopenia, trombocitopenia y otros cambios en el recuento sanguíneo. Estas reacciones adversas, normalmente desaparecen al terminar el tratamiento. Alteraciones en la coagulación, anemia hemolítica, Shock anafiláctico, enfermedad del suero, hepatitis, ictericia colestásica, aumento de la creatinina en suero, nefritis intersticial. Se recomienda precaución en pacientes tratados simultáneamente con diuréticos y/o otros medicamentos potencialmente nefrotóxicos, especialmente en aquellos pacientes que padecen enfermedades subyacentes en las que puede producirse isquemia renal. Debido al uso simultáneo de estos medicamentos, puede producirse deficiencia en la función renal o incluso fallo renal agudo. En estos casos, es necesaria la monitorización de la función
i. SOBREDOSIS:
Dada la escasa toxicidad de la cefixima, no es previsible que la ingestión masiva accidental dé lugar a un cuadro de intoxicación, recomendándose en estos casos lavado gástrico y tratamiento sintomático. En caso de manifestaciones alérgicas importantes el tratamiento debe ser sintomático, adrenalina, corticoides, antihistamínicos. La hemodiálisis o la diálisis peritoneal no son medidas adecuadas para eliminar cantidades relevantes de cefixima.
DATOS FARMACÉUTICOS
a. INCOMPATIBILIDADES:
No se han descrito
b. PERIODO DE VALIDEZ:
3 años
b. PRECAUCIONES ESPECIALES DE CONSERVACIÓN:
Almacenar a temperatura no mayor de 30°C
d. NATURALEZA Y CONTENIDO DEL ENVASE:
Farmacia:
Caja con frasco para 50 mL de suspensión reconstituida.
Caja con frasco para 100 mL de suspensión reconstituida.
Muestra Médica:
Caja con frasco para 20 mL de suspensión reconstituida. (No aplica para Costa Rica)
FECHA DE REVISIÓN
Mayo – 2019
REFERENCIAS BIBLIOGRÁFICAS
Agencia Española de Medicamentos. https://cima.aemps.es/cima/dochtml/ft/59733/ FichaTecnica_59733.html.