Forma Farmacéutica y Formulación
Forma Farmacéutica
Aerosol (Spray)
Presentación
Cada 30 gramos contiene:
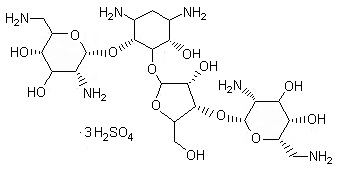
Neomicina Sulfato eq. A neomicina…150.00 mg
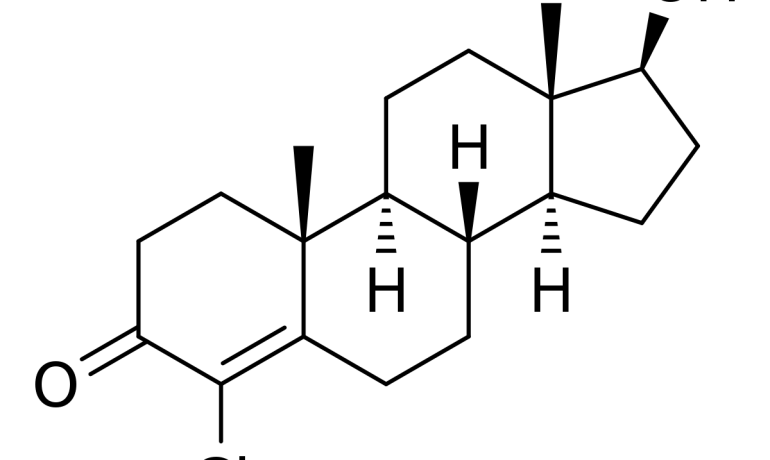
Clostebol Acetato eq. A clostebol…150.00 mg
Excipientes c.s.p.
DATOS CLÍNICOS
a. INDICACIONES TERAPÉUTICAS:
Neobol® Aerosol está indicado en enfermedades de la piel y mucosas como: infecciones en la piel, úlcera cutánea, quemaduras, heridas y dermatosis2, 3.
B. POSOLOGÍA Y FORMA DE ADMINISTRACIÓN:
Posología
Aplicar una fina capa del producto sobre la lesión 1 ó 2 veces por día. La región puede cubrirse con una gasa estéril1.
Forma de administración
Vía de administración: Tópica2, 3.
C. CONTRAINDICACIONES:
Contraindicado en pacientes con hipersensibilidad2, 3 a neomicina sulfato, clostebol acetato y a cualquiera de los excipientes del producto1.
D. ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE EMPLEO:
Debe evitarse el uso continuo de Neobol® Aerosol.
Debido al riesgo potencial de ototoxicidad y nefrotoxicidad de la neomicina, no se recomienda el uso prolongado del producto en superficies lesionadas extensas que puedan permitir la absorción de neomicina1, 2, 3.
Evitar la aplicación en ojos y la inhalación. No exponer a temperaturas elevadas, ni vaporizar cerca del fuego. No perforar ni quemar después de su uso. Se recomienda agitar antes de su uso, no vaporizar en llamas o cuerpos incandescentes1.
No utilizar durante el parto1. Población Pediátrica
El uso continuo de Neobol® Aerosol debe evitarse; especialmente en la primera infancia1.
Información importante sobre excipientes
Este medicamento puede causar reacciones en la piel.
Contiene aceite de ricino. El contacto prolongado o repetido con la piel puede producir dermatitis5.
E. INTERACCIONES CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN:
El uso combinado de Neobol® Aerosol con preparaciones tópicas que contienen otros antibióticos aminoglucósidos puede aumentar el riesgo de sensibilización o potenciar los efectos secundarios1.
F. EMBARAZO Y LACTANCIA
Durante el embarazo y la lactancia, el medicamento solo se debe administrar si realmente es necesario1.
G. EFECTOS SOBRE LA CAPACIDAD DE CONDUCIR Y MANEJAR MAQUINARIA
La administración cutánea de Neobol® Aerosol no afecta la capacidad para conducir y utilizar maquinaria1.
H. REACCIONES ADVERSAS
El uso, especialmente si es prolongado, del producto puede dar lugar a fenómenos de sensibilización1, 2, 3.
Además, una aplicación prolongada durante varias semanas en áreas extensas de tejidos dañados podría dar lugar a la aparición de efectos sistémicos, como hipertricosis debido a una absorción masiva de clostebol1.
Después de su aplicación local, en 6 a 8% de los enfermos hay reacciones de hipersensibilidad y en particular erupciones cutáneas. Las personas sensibles al medicamento pueden mostrar reacciones cruzadas cuando entran en contacto con otros aminoglucósidos. Los efectos tóxicos más importantes de la neomicina son daño renal y sordera por ataque del VIII par, ambos cuadros son más frecuentes cuando se utilizan cantidades relativamente grandes del antibiótico por vía parenteral. He aquí la explicación de que se le haya dejado de utilizar por estas vías. La toxicidad también ha ocurrido en sujetos con función normal renal después de aplicación local o lavado de heridas con una solución de neomicina al 0.5%. Se ha sabido de casos de bloqueo neuromuscular y parálisis respiratoria después de lavado de heridas o cavidades serosas. Los efectos adversos más importantes después de ingerir neomicina son malabsorción intestinal e infecciones sobreañadidas. Las personas que ingieren 4 a 6 g del fármaco al día presentan a veces un síndrome similar al del esprue que incluye diarrea, esteatorrea y azotorrea. Se observa a veces proliferación excesiva de levaduras en el intestino; en muchos casos no se acompaña de diarrea o de otros síntomas. La ingestión de dosis todavía mayores de neomicina casi nunca tiene efecto alguno en los valores sanguíneos de protrombina3.
La administración tópica en la piel lesionada puede producir sordera parcial o total irreversible4.
I. SOBREDOSIFICACIÓN
Una eventual sobredosis puede contemplarse solo en el caso de aplicaciones prolongadas y en áreas grandes de piel lesionada, lo que podría inducir efectos secundarios como sensibilización1.
Tratamiento
Suspender el tratamiento1.
PROPIEDADES FARMACOLÓGICAS
A. PROPIEDADES FARMACODINÁMICAS
Mecanismo de acción:
De los dos ingredientes activos de Neobol® Aerosol, el acetato de clostebol, un derivado de la testosterona, ejerce un efecto de curación trófica y causa un marcado acortamiento del tiempo de reparación de las lesiones cutáneas y cutáneo-mucosas. Este efecto se debe a la propiedad común de todos los esteroides anabolizantes para activar los mecanismos bioquímicos celulares delegados a la síntesis de proteínas, es decir, la formación del material de construcción más importante del que dependen los procesos de granulación y reepitelización. El segundo componente de Neobol® Aerosol, la neomicina, actúa indirectamente en el mismo proceso, favoreciendo la eliminación o previniendo la aparición de una infección local, que es notoriamente el factor más importante de retraso en la evolución de la cicatrización de las heridas1.
B. PROPIEDADES FARMACOCINÉTICAS
Absorción
En vía tópica, el acetato de clostebol muestra muy poca absorción sistémica1.
C. DATOS PRECLÍNICOS SOBRE SEGURIDAD
Las pruebas de toxicidad subaguda realizadas en conejos para aplicación local repetidas durante 15 días con una dosis de 1g/kg han excluido las variaciones en el peso corporal, el consumo de alimentos y agua, la diuresis, la urea en sangre y bilirrubinemia, así como el peso de los órganos internos. La piel de los animales tratados presenta alteraciones locales de una cantidad significativamente menor en comparación con la tratada con los excipientes solos1.
DATOS FARMACÉUTICOS
A. LISTA DE EXCIPIENTES
Aceite de ricino
Propelentes:
Etano
Propano
Isobutano
N-butano
Isopentano
B. INCOMPATIBILIDADES
No procede
C. PERÍODO DE VALIDEZ
36 meses
D. PRECAUCIONES ESPECIALES DE CONSERVACIÓN
Se debe conservar en condiciones de temperatura menor de 30 °C y alejado del calor excesivo.
NATURALEZA Y CONTENIDO DEL EMPAQUE
Lata de aluminio con tapa plástica blanca empacado en caja de cartón.
Presentaciones
- Muestra Médica: caja de cartón conteniendo una lata con 30
- Farmacia: caja de cartón conteniendo una lata con 30
REFERENCIAS BIBLIOGRÁFICAS
- Agenzia Italiana del Farmaco:
- https://farmaci.agenziafarmaco.gov.it/aifa/servlet/PdfDownloadServlet?pdfFileNa me=footer_000143_020942_RCP.pdf&retry=0&sys=m0b1l3
- Agenzia Italiana del Farmaco:
- https://farmaci.agenziafarmaco.gov.it/aifa/servlet/PdfDownloadServlet?pdfFileNa me=footer_000143_020942_FI.pdf&retry=0&sys=m0b1l3
- Goodman & Gilman (2001). Las Bases Farmacológicas de la Terapéutica. 10a. edición. McGRAW HILL INTERAMERICANA, México. Pág. 1252-1253.
- Sweetman S. et al. (2002). Martindale, Guía Completa de Consulta Farmacoterapéutica. 33a. edición. PHARMA EDITORES, Londres, Gran Bretaña. Pág. 347-348,
- Instituto Nacional de Seguridad y Salud en el Trabajo (INSST). http://www.insht.es/InshtWeb/Contenidos/Documentacion/FichasTecnicas/FISQ/F icheros/1401a1510/nspn1452.pdf
- Revisión del texto: Mayo de 2019
- Versión: 4